【秒懂】不同类型的口罩、防护服怎样出口到欧盟和美国?
突如其来的疫情,让口罩、防护服在全球市场范围内供不应求。本文重点介绍口罩、防护服的分类以及“跨界”的生产制造商怎样以最快速度完成认证进入欧盟和美国市场。
l 口罩
口罩按其预期用途,分为:个人防护口罩和医用口罩两大类别。不同的类别在各国依据不同的法规管理,进入市场前的要求也不一样。所以制造商首先要确定自己产品的预期用途即类别。
01个人防护 口罩
欧盟 PPE
口罩需依据欧洲个人防护法规PPE (Personal Protective Equipment) Regulation (EU) 2016/425实施申请,口罩主要分类FFP2、FFP3。欧盟针对防护口罩的专用标准是EN149.
企业需选择有PPE法规授权的公告机构(Notified body)实施申请,NB机构需审核企业质量管理体系和CE技术文档。审核通过后可获得PPE法规的CE证书。
美国NIOSH
NIOSH: National Institute for Occupational Safety and Health美国国家职业安全卫生研究所。
根据联邦法规42 CFR Part 84,NIOSH将其认证的防颗粒物口罩根据中间过滤网特性(N系列、R系列、P系列)和过滤材质的最低过滤效率(95%、99%、99.97%)组合分为N100, N99, N95, R100, R99, R95, P100, P99, P95共9种。
上述9种口罩需满足美国联邦法规42 CFR Part 84的要求,主要测试指标包括呼气阻力测试(Exhalation Resistance Test)、呼气阀泄漏测试(Exhalation Valve Leakage Test)、吸气阻力测试(Inhalation Resistance Test)、过滤效率match测试(Sodium Chloride Test)。
具体的测试则由NIOSH下属的NPPTL (National Personal Protective Technology Laboratory)实验室操作。
【认证申请】需按照NIOSH的指南实施,企业需寄送样品至NIOSH实验室实施测试,同时提交技术性资料(包括质量体系部分资料)至NIOSH文审,只有文审和测试都通过,NIOSH才核发批文。
02医用口罩
欧盟 CE / MDR
依据Regulation(EU)2017/745 on medical devices即MDR;Annex VIII分类规则10,Class Is,需要公告参与审核体系ISO13485:2016及CE技术文件。
由于欧盟采用的是委托具备资质的第三方公告机构的监管方式,审核并颁发证书,相关费用以机构报出的为准,鉴于MDR实施不久,认证周期无法固定判断,依据MDD的经验,预计12-15个月左右。
欧盟有医疗口罩专标EN 14683-2014:
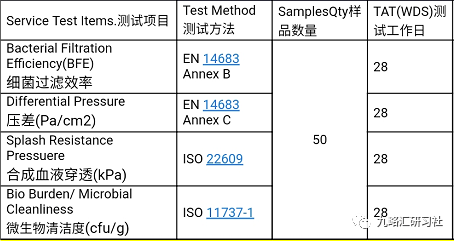
为了应对当下继续出口的情况,建议企业准备ISO13485 认证,并按照一类非无菌Class I方式进行编写MDR技术文档,准备自我声明;选择欧代,进行欧盟注册;加贴CE标识,出口欧盟。
美国 FDA
依据美国FDA分类:
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfPCD/classification.cfm 选择关键词" Mask ",进行搜索:
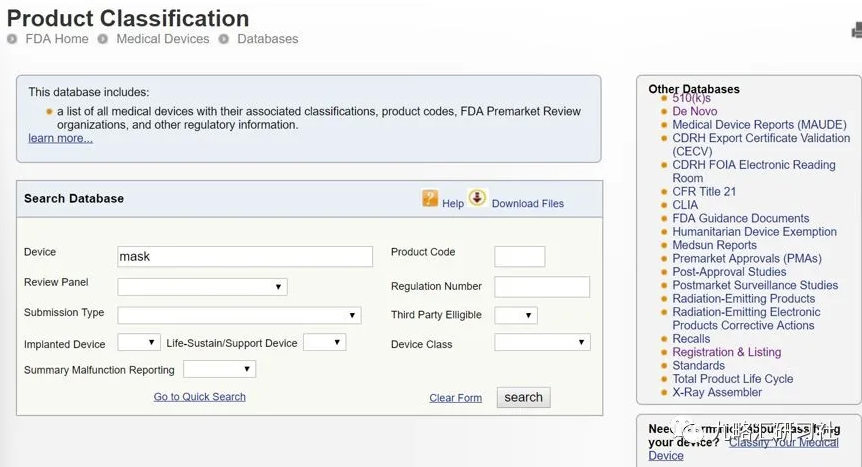
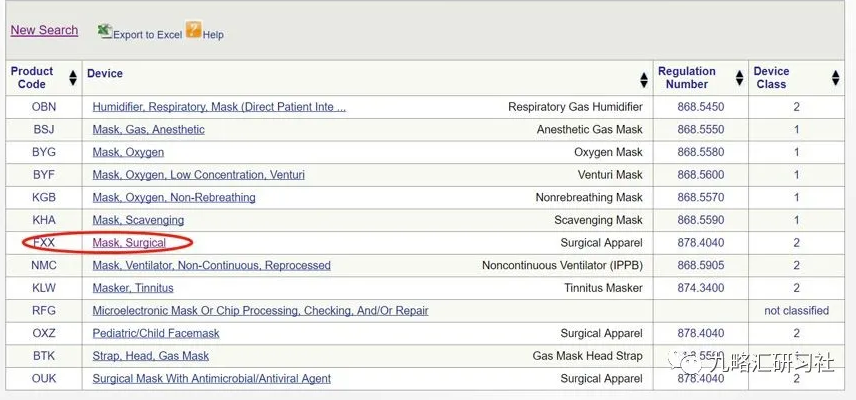
选择最合适的代码:FXX
依据FDA指南编写510k报告,提交美国FDA审批。
【认证申请的其他要求】
1.产品的性能测试包括:
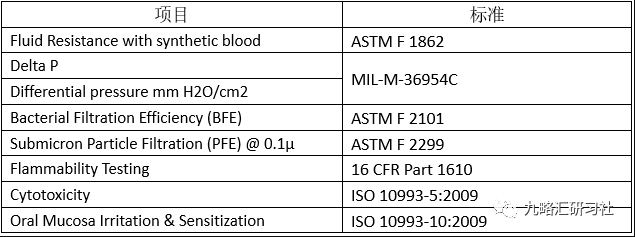
2.美国FDA 510k审核费,2020年正常官方费用:$11,594,小规模企业可申请优惠:$2,899。
&nbs
曝光台
-
【天津】虚假检验报告!一检测公司被罚32万元
2020-03-09 我要测
-
【海南】3家认证机构拟被立案调查
2020-03-09 质量与认证
-
警示 | 涉案违法所得超30万,一检测机构被追究刑事责任
2020-03-09 质量与认证
-
严惩弄虚作假 | 一批出具虚假检验报告典型案例公布
2020-03-09 质量与认证
-
警示 | 一认证机构被罚5万
2020-03-09 质量与认证
-
最高罚款32万并吊销资质!六类虚假检验报告典型案例公布
2020-03-09 质量与认证
-
罚款 | 摆拍现场照片、伪造审核会议签到表,一认证机构被罚6万
2020-03-09 质量与认证
-
警钟长鸣:出具虚假报告结果—判刑、罚款、禁止从业,授权签字人终身负责!
2020-03-09 陕西省质量认证认可协会
-
别用!这些头盔质量不合格
2020-03-09 中国质量新闻网
-
撤销 | 19名审核员注册资格
2020-03-09 质量与认证
-
处罚 | 一检测机构被罚6万,2名当事人被罚
2020-03-09 质量与认证
-
处罚 | 北京一认证机构被罚8万
2020-03-09 质量与认证
-
撤销 | 多次出具虚假、超范围检验检测报告,山西一家环境检测公司证书被撤销
2020-03-09 山西省市场监督管理局
-
通报 | 18家检测机构涉嫌严重违法违规
2020-03-09 湖南省市场监督管理局
-
涉嫌违法!刘媛媛、徐杉Sherry等知名网红主播双十一直播带货广告被查
2020-03-09 中国质量新闻网